Возможности применения коллагенотерапии для реабилитации после пластической хирургии
СкачатьРМЖ. Медицинское обозрение. T. 9, №6, 2025
Опубликовано в журнале РМЖ
Авторы: О.Б. Борзых , М.М. Петрова , Н.А. Шнайдер, С.В. Данилова
Резюме
Возникновение гипертрофических рубцов представляет особую проблему после пластической хирургии. Одним из перспективных методов контроля и улучшения репарации раны является применение коллагена. Ранее на модели ишемизированной раны у экспериментальных животных была показана эффективность клинического применения медицинского изделия на основе нативного коллагена I типа. Коллаген действует как естественный субстрат для прикрепления клеток, он может опосредовать множество физиологических взаимодействий, способствующих регенерации во время сложного процесса заживления ран, начиная от ангиогенеза и заканчивая реэпителизацией. В работе приведены 2 клинических наблюдения применения медицинского изделия на основе нативного коллагена I типа для контроля и улучшения заживления посттравматической и послеоперационной раны. У пациентки с посттравматической раной отмечено ускорение заживления раны с формированием нормотрофического малозаметного рубца. У пациентки с послеоперационной раной отмечен контроль и улучшение заживления гипертрофического рубца. Показана эффективность применения медицинского изделия на основе нативного коллагена I типа.
Введение
Одно из фундаментальных свойств всех организмов — это способность тканей к их восстановлению после повреждения.[1] У взрослых людей, в отличие от плода (до 24 нед. гестации), кожные раны заживают в виде рубцов.[2] В рубцовой ткани снижается биомеханическая и физиологическая функциональность из-за изменения клеточного состава и строения внеклеточного матрикса, в частности изменения строения и расположения коллагеновых волокон.[3] Репарация раны — хорошо организованный процесс с участием клеточных и внеклеточных компонентов.[4] При этом клетки формируют внеклеточный матрикс, а внеклеточный матрикс активно контролирует форму, поведение и функции клеток. Поэтому внеклеточный матрикс играет фундаментальную роль в точно регулируемом восстановлении тканей у взрослых людей и является ключевым элементом, определяющим эффективность и степень выраженности процесса восстановления.[5] Взаимодействие фибробластов с внеклеточным матриксом осуществляется по типу аутокринной регуляции, которая имеет решающее значение в процессе заживления ран. Фибробласт должен постоянно создавать новые матриксные белки для надлежащего заживления кожной раны, одновременно регулируясь белками собственного производства.[6] Можно выделить следующие факторы, формирующие гипертрофические и келоидные рубцы: чрезмерная выработка коллагена и других компонентов внеклеточного матрикса; потеря или подавление ключевых стоп-сигналов; дисфункция в разрешении и подавлении деградирующих ферментов, участвующих в ремоделировании грануляционной ткани.[5]
Частота развития гипертрофических рубцов, по данным разных авторов, варьирует от 15 до 70% после хирургических вмешательств.[7–9] Одним из важных факторов прогнозирования гипертрофических рубцов является время полного заживления: уменьшение времени снижает вероятность гипертрофических рубцов.[10] Ранее основные исследования по заживлению ран были больше сконцентрированы на клеточном компоненте, новые исследования отводят центральное место внеклеточному матриксу в управлении фенотипами клеток в процессе репарации.[11]
В настоящее время предложено множество способов для контроля и улучшения заживления после повреждения кожи, включая применение инвазивных (инъекции тромбоцитарной плазмы, ботулинического токсина типа А, глюкокортикостероидов (ГКС), 5-фторурацила, интерферона и блеомицина) и неинвазивных методов (лазерная терапия, кремы с факторами роста и цитокинами, силиконами).[10, 12, 13] Однако «золотого стандарта» на сегодняшний день нет, что связано как с неполным представлением о точке приложения разных методов и недостатком проспективных исследований, так и с некоторыми побочными эффектами применения препаратов. Так, применение ГКС может привести к боли и атрофии окружающих тканей, телеангиоэктазиям, остеопорозу. Ряд авторов считают, что они должны быть отнесены к препаратам второй линии (когда более простые методы неэффективны).[14, 15]
Компоненты внеклеточного матрикса кожи обеспечивают взаимодействие между различными клетками из-за своего специфического трехмерного расположения. Такое взаимодействие влияет на прикрепление, миграцию, дифференциацию и морфогенетические признаки. Нарушение структуры внеклеточного матрикса снижает его регулирующую и репарационную роль, что приводит к нарушению рубцевания.[16] Одним из перспективных методов контроля и улучшения репарации раны является применение коллагена. Так, на ранних сроках заживления ран коллаген способствует интенсивной пролиферации стволовых клеток эпидермиса и фибробластов с дальнейшей обратимой дифференцировкой фибробластов в миофибробласты, способствуя сужению раны. Также было показано, что коллаген стимулирует миграцию клеток и ускоряет заживление. При гистологическом исследовании было отмечено, что на 8-й день в группе с применением коллагена обнаружено меньше воспалительных клеток, а к 13-му дню — больший ангиогенез (в сравнении с группой с применением физиологического раствора).[17]
Коллаген действует как естественный субстрат для прикрепления клеток, он может опосредовать множество физиологических взаимодействий, способствующих регенерации, во время сложного процесса заживления ран, начиная от ангиогенеза и заканчивая реэпителизацией.[18]
Примерами препаратов на основе нативного коллагена являются медицинские изделия, содержащие коллаген I типа нативный нереконструированный, — COLLOST® гель 7 и 15% («БиоФАРМАХОЛДИНГ», Россия), на основе фибрилл коллагена.[19] Далее мы рассмотрим клинические наблюдения применения данного препарата у пациенток на разных стадиях заживления раны после травмы и после оперативного вмешательства (письменное согласие пациенток на публикацию получено).
Клиническое наблюдение 1
Пациентка, 41 год, обратилась с рваной раной лба после тупой травмы (рис. 1). Хирургом был наложен шов. На второй день после травмы (рис. 2) было инъецировано медицинское изделие, содержащие коллаген I типа нативный нереконструированный 7%, по краям раны и вдоль шва.

Рис. 1. Пациентка, 41 год, с рваной раной лба после тупой травмы

Рис. 2. Второй день после травмы перед введением медицинского изделия, содержащего коллаген I типа нативный нереконструированный: стадия воспаления заживающей раны
На 17-е сутки после травмы видна образовавшаяся грануляционная ткань без признаков избыточного воспаления (рис. 3). Была выполнена 2-я процедура введения медицинского изделия по краям и в центре заживающей раны для создания условий миграции фибробластов. На 34-е сутки после травмы рана находится в стадии ремоделирования: образовавшаяся ранее грануляционная ткань замещается постоянным матриксом (рис. 4).
Была выполнена 3-я процедура введения медицинского изделия, содержащего коллаген I типа нативный нереконструированный, по краям и в центре заживающей раны.
В настоящее время проведено 4 процедуры лечения раны медицинским изделием, содержащим коллаген I типа нативный нереконструированный. При осмотре раны через 3,5 мес. после получения травмы (перед 4-й процедурой) отмечено значительное улучшение состояния раны без признаков воспаления, цвет близкий к окружающим тканям (рис. 5). В настоящее время пациентка находится под наблюдением.
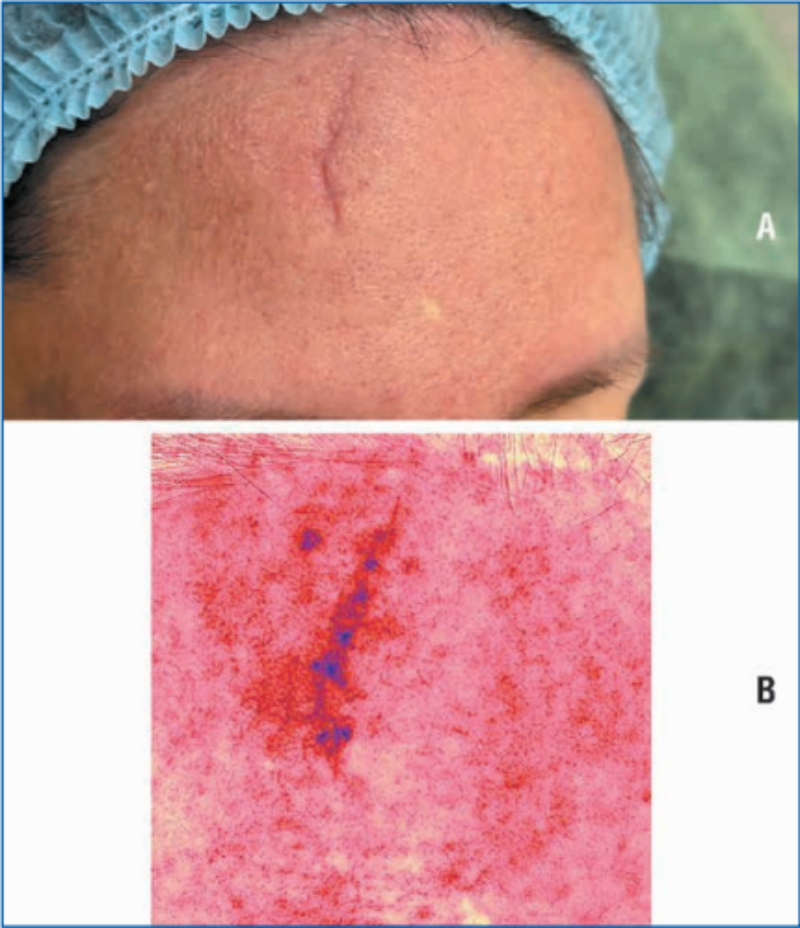
Рис. 3. 17-й день после травмы перед введением медицинского изделния, содержащего коллаген I типа нативный нереконструированный: стадия пролиферации заживающей раны. А — фото раны; B — отображение сосудистого компонента раны на аппарате Antera 3D
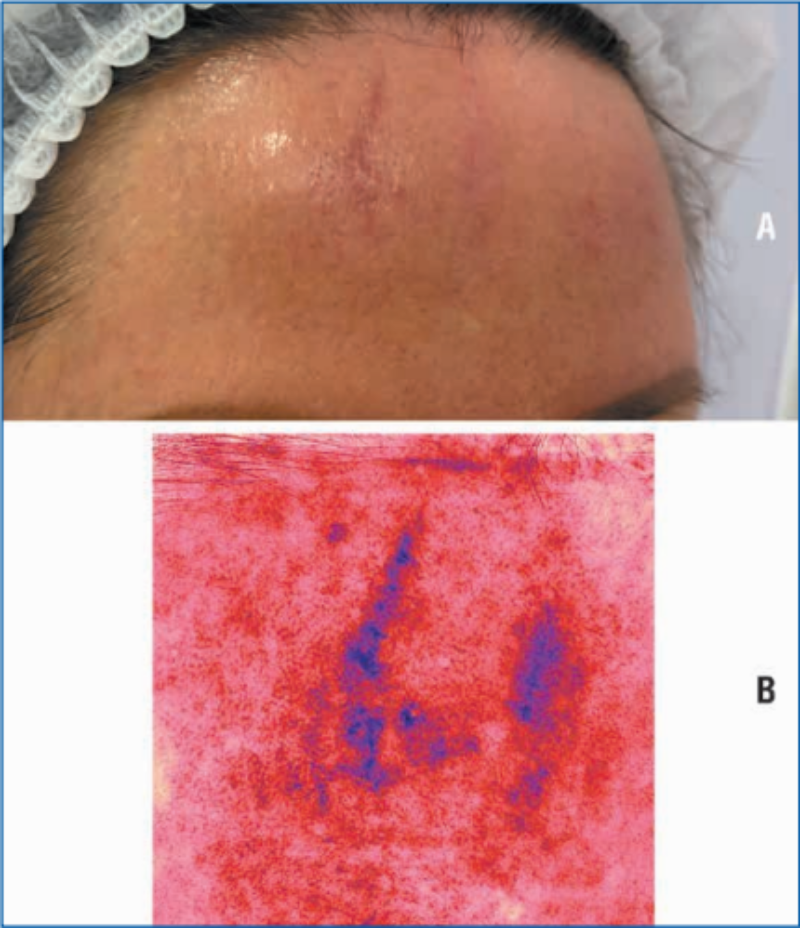
Рис. 4. 34-й день после травмы перед введением медицинского изделия, содержащего коллаген I типа нативный нереконструированный: стадия ремоделирования заживающей раны. А — фото раны; B — отображение сосудистого компонента раны на аппарате Antera 3D
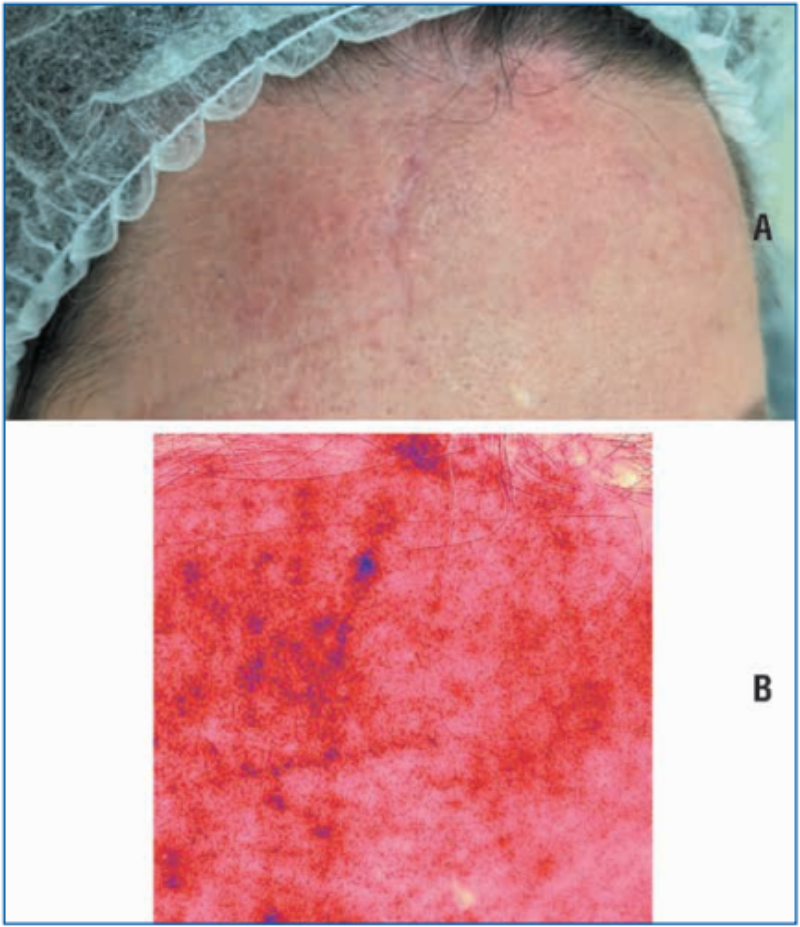
Рис. 5. Через 3,5 мес. после травмы перед введением медицинского изделия, содержащего коллаген I типа нативный нереконструированный: стадия ремоделирования заживающей раны. А — фото раны; B — отображение сосудистого компонента раны на аппарате Antera 3D
Клиническое наблюдение 2
Пациентка, 36 лет, через 3 мес. после абдоминопластики обратилась с жалобами на зуд, «стягивание» и уплотнение в области послеоперационного рубца (рис. 6). Пациентке было инъецировано медицинское изделие, содержащее коллаген I типа нативный нереконструированный 15%, интрарубцово на протяжении всего рубца. Через неделю пациентка отметила отсутствие зуда и ощущения «стягивания» в области рубца. При осмотре через 3 нед. отмечено уменьшение плотности рубца и небольшое снижение интенсивности покраснения (рис. 7). Через 3 нед. после 1-й процедуры было выполнено следующее введение медицинского изделия, содержащего коллаген I типа нативный нереконструированный 7%, еще через 3 нед. выполнена 3-я процедура введения медицинского изделия, содержащего коллаген I типа нативный нереконструированный 7% (рис. 8), и через 4 мес. после начала лечения (рис. 9) проведена 4-я процедура введения медицинского изделия, содержащего коллаген I типа нативный нереконструированный 7%. При осмотре через 4 мес. после начала лечения отмечено значительное улучшение состояния рубца: снижение плотности, уменьшение интенсивности окраски. В настоящее время пациентка находится под наблюдением.
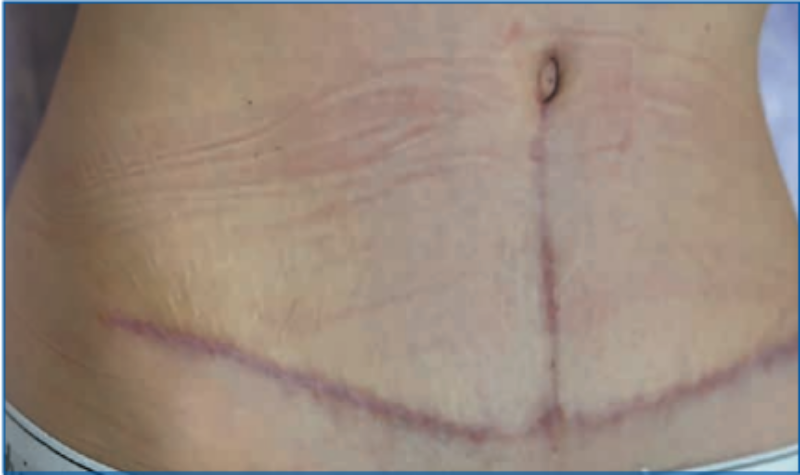
Рис. 6. Пациентка, 36 лет, через 3 мес. после абдоминопластики
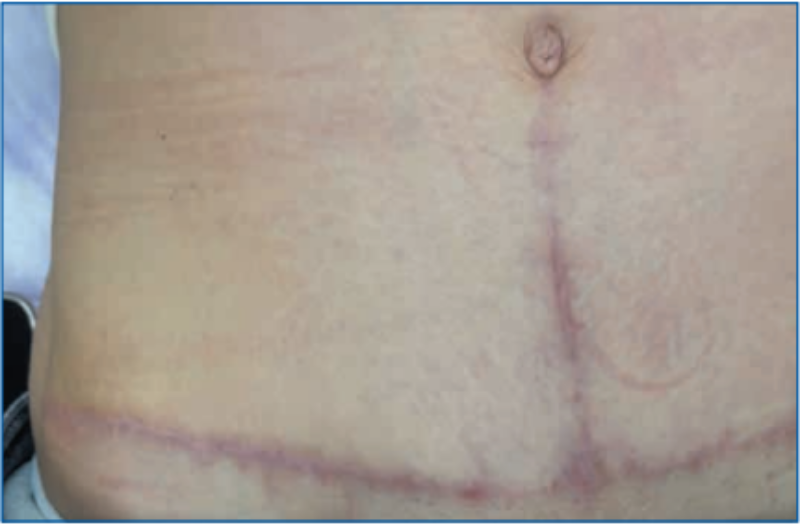
Рис. 7. Пациентка, 36 лет, через 4 мес. после абдоминопластики и 3 нед. после 1-й процедуры коллагенотерапии медицинским изделием, содержащим коллаген I типа нативный нереконструированный 15%
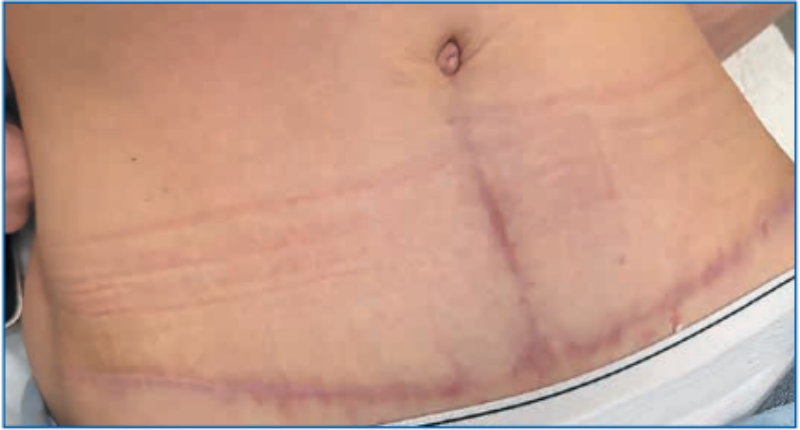
Рис. 8. Пациентка, 36 лет, через 4,5 мес. после абдоминопластики и 6 нед. после начала коллагенотерапии
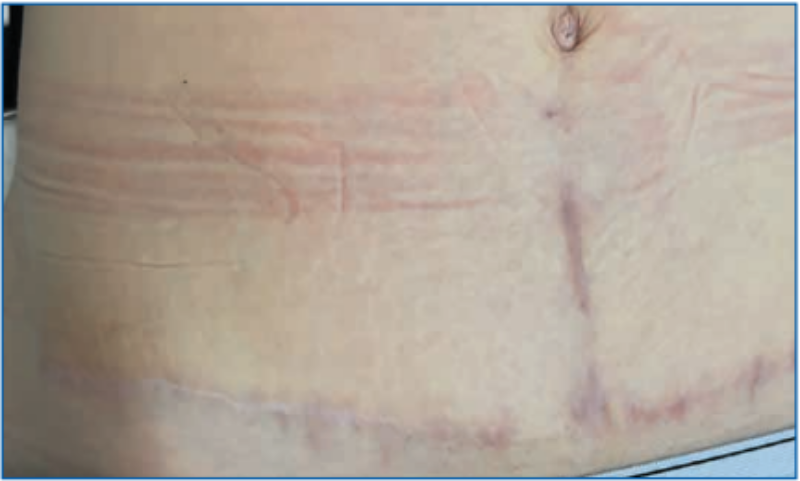
Рис. 9. Пациентка, 36 лет, через 7 мес. после абдоминопластики и 4 мес. после начала коллагенотерапии
Обсуждение
Проблема гипертрофических рубцов остается чрезвычайно актуальной. Несмотря на большое количество работ по данной тематике, единого «золотого стандарта» лечения и профилактики нет. Однако можно отметить смещение фокуса внимания с применения ГКС (как монотерапии) в сторону методик, в целом улучшающих регенерацию, а также переключение основного внимания с клеточных компонентов процесса репарации в сторону внеклеточного матрикса.[10–15] Одним из относительно новых направлений тактики ведения пациентов является применение инъекционных медицинских изделий на основе коллагена. На клеточных культурах (в присутствии коллагена) была показана стимуляция миграции клеток, ускорение заживления, менее выраженное воспаление и более эффективный ангиогенез.[17] В другом исследовании на модели экспериментальных животных (крысы) было показано снижение выраженности воспаления, улучшение ангиогенеза и уменьшение сроков репарации при внутрикожном введении и введении в полость раны медицинского изделия COLLOST® гель 7%.[20]
В представленных клинических наблюдениях отмечена эффективность применения медицинского изделия COLLOST® гель 7 и 15% на разных сроках после операции и после травмы. Данные экспериментального исследования на животных не могут полностью служить обоснованием использования изделия у человека. Однако медицинское изделие COLLOST® гель 7% имеет большую доказательную базу применения у пациентов, по данным исследований было отмечено улучшение состояния внеклеточного матрикса.[21, 22] В любом случае возможность применения коллагенотерапии для улучшения репарации кожи после хирургических вмешательств нуждается в дополнительных исследованиях для создания четких алгоритмов применения.
Заключение
Коллаген служит основным компонентом внеклеточного матрикса кожи. Он участвует в ряде физиологических процессов, способствующих регенерации в ходе сложного процесса заживления ран. Применение коллагена является перспективным направлением исследований в сфере регенерации ран в связи с рядом преимуществ. Так, применение коллагена не связано с побочными эффектами, наблюдаемыми при использовании ГКС (боль и атрофия кожи, телеангиоэктазии). Также применение коллагена действует не только на рубцовую ткань, но и улучшает регенерацию окружающих тканей. Дополнительным преимуществом является доступность препарата в сравнении с новейшими разработками в сфере заживления ран (генно-модифицированные технологии, использование стволовых клеток и др.). В клинических наблюдениях продемонстрирована эффективность применения препаратов на основе нативного коллагена для контроля и улучшения заживления ран после травмы и операции.
Литература
- Mostaço-Guidolin L., Rosin N.L., Hackett T.L. Imaging Collagen in Scar Tissue: Developments in Second Harmonic Generation Microscopy for Biomedical Applications. Int J Mol Sci. 2017;18(8):1772. DOI: 10.3390/ijms18081772
- Karppinen S.M., Heljasvaara R., Gullberg D. et al. Toward understanding scarless skin wound healing and pathological scarring. F1000Res. 2019;8:F1000 Faculty Rev-787. DOI: 10.12688/f1000research.18293.1
- Knoedler S., Broichhausen S., Guo R. et al. Fibroblasts — the cellular choreographers of wound healing. Front Immunol. 2023;14:1233800. DOI: 10.3389/fimmu.2023.1233800
- Ud-Din S., Volk S.W., Bayat A. Regenerative healing, scar-free healing and scar formation across the species: current concepts and future perspectives. Exp Dermatol. 2014;23(9):615–619. DOI: 10.1111/exd.12457
- Stoica A.E., Grumezescu A.M., Hermenean A.O. et al. Scar-Free Healing: Current Concepts and Future Perspectives. Nanomaterials (Basel). 2020;10(11):2179. DOI: 10.3390/nano10112179
- Tracy L.E., Minasian R.A., Caterson E.J. Extracellular Matrix and Dermal Fibroblast Function in the Healing Wound. Adv Wound Care (New Rochelle). 2016;5(3):119–136. DOI: 10.1089/wound.2014.0561
- Leszczynski R., da Silva C.A., Pinto A.C.P.N. et al. Laser therapy for treating hypertrophic and keloid scars. Cochrane Database Syst Rev. 2022;9(9):CD011642. DOI: 10.1002/14651858.CD011642.pub2
- Gauglitz G.G., Korting H.C., Pavicic T. et al. Hypertrophic scarring and keloids: pathomechanisms and current and emerging treatment strategies. Mol Med. 2011;17(1–2):113–125. DOI: 10.2119/ molmed.2009.00153
- Lewis W.H., Sun K.K. Hypertrophic scar: a genetic hypothesis. Burns. 1990;16:176–178. DOI: 10.1016/0305-4179(90)90033-s
- Shirakami E., Yamakawa S., Hayashida K. Strategies to prevent hypertrophic scar formation: a review of therapeutic interventions based on molecular evidence. Burns Trauma. 2020;8:tkz003. DOI: 10.1093/burnst/tkz003
- Wells A., Nuschke A., Yates C.C. Skin tissue repair: Matrix microenvironmental influences. Matrix Biol. 2016;49:25–36. DOI: 10.1016/j.matbio.2015.08.001
- Bi M., Sun P., Li D. et al. Intralesional Injection of Botulinum Toxin Type A Compared with Intralesional Injection of Corticosteroid for the Treatment of Hypertrophic Scar and Keloid: A Systematic Review and Meta-Analysis. Med Sci Monit. 2019;25:2950–2958. DOI: 10.12659/MSM.916305
- Murdock J., Sayed M.S., Tavakoli M. et al. Safety and efficacy of a growth factor and cytokine-containing topical product in wound healing and incision scar management after upper eyelid blepharoplasty: a prospective split-face study. Clin Ophthalmol. 2016;10:1223–1228. DOI: 10.2147/OPTH.S109517
- Zhang T., Wang X.F., Wang Z.C. et al. Current potential therapeutic strategies targeting the TGF-β/Smad signaling pathway to attenuate keloid and hypertrophic scar formation. Biomed Pharmacother. 2020;129:110287. DOI: 10.1016/j.biopha.2020.110287
- Gauglitz G.G. Management of keloids and hypertrophic scars: current and emerging options. Clin Cosmet Investig Dermatol. 2013;6:103–114. DOI: 10.2147/CCID.S35252
- Urciuolo F., Casale C., Imparato G., Netti P.A. Bioengineered Skin Substitutes: the Role of Extracellular Matrix and Vascularization in the Healing of Deep Wounds. J Clin Med. 2019;8(12):2083. DOI: 10.3390/jcm8122083
- Liu T., Hao J., Lei H. et al. Recombinant collagen for the repair of skin wounds and photo-aging damage. Regen Biomater. 2024;11:rbae108. DOI: 10.1093/rb/rbae108
- Davison-Kotler E., Marshall W.S., García-Gareta E. Sources of Collagen for Biomaterials in Skin Wound Healing. Bioengineering (Basel). 2019;6(3):56. DOI: 10.3390/bioengineering6030056
- Потекаев Н.Н., Борзых О.Б., Карпова Е.И. и др. Патогенетические аспекты использования основных методов эстетической медицины при инволюционных изменениях кожи. Русский медицинский журнал. 2022;8:48–54.
Potekaev N.N., Borzykh O.B., Karpova E.I. et al. Pathogenetic aspects concerning the usage of the main methods in aesthetic medicine for involutional skin changes. RMJ. 2022;8:48–54 (in Russ.). - Андреев-Андриевский А.А., Болгарина А.А., Манских В.Н. и др. Механизмы ранозаживляющего действия нативного коллагена I типа в модели ишемизированных полнослойных ран кожи на примере медицинского изделия «Коллост» (часть I). Хирургия. Журнал им. Н.И. Пирогова. 2020;10:79–87. DOI: 10.17116/hirurgia202010179.
Andreev-Andrievsky A.A., Bolgarina A.A., Manskih V.N. et al. Mechanisms of the wound-healing action of native collagen type I in ischemic model full-thickness skin wounds on the example — medical devices Collost (part I). Pirogov Russian Journal of Surgery. 2020;3:79–87 (in Russ.). DOI: 10.17116/hirurgia202010179 - Мантурова Н.Е., Стенько А.Г., Петинати Я.А. и др. Инъекционный коллаген в коррекции возрастных изменений кожи: экспериментально-клинические параллели. Вестник РГМУ. 2019;1:78–85. DOI: 10.24075/vrgmu.2019.010
Manturova N.E., Stenko A.G., Petinati Ya.A. Injectable collagen in correction of age-related skin changes: experimental and clinic parallels. Bulletin of RSMU. 2019;1;78–85 (in Russ.). DOI: 10.24075/vrgmu.2019.010 - Potekaev N.N., Borzykh O.B., Karpova E.I. et al. A New Approach toward the Management of Patients with Premature Skin Aging Using the Predictor Effect. Cosmetics. 2023;10(2):49. DOI: 10.3390/cosmetics10020049